Beyin kanserinin agresif bir türündeki tümör hücrelerini öldüren küçük altın nanopartiküllerin kullanımını içeren “Trojan atı” tedavisi bilim insanları tarafından başarıyla test edildi.
Çığır açan teknik sayesinde sonunda yetişkinlerde en sık görülen ve agresif beyin tümörü olarak tedavisinin zorluğunun bilindiği çoklu glioblastoma tedavi edilebilecek. Bu hastalığı teşhisten birkaç ay sonra hastaların çoğunun vefat etmektedir ve sadece 100 kişiden 6’sı 5 yıl sonra yaşamına devam etmektedir.
Araştırma hem altın hem de geleneksel bir kanser ilacı olan sisplatin içeren nano yapıların üretilmesini sağlamıştır. Glioblastoma hastalarından alınıp laboratuvarda büyütülen tümör hücrelerine bu nano yapılar salındı.
Daha sonra tümör hücresinin içine alınan bu “nano küreler” radyoterapiye maruz bırakıldı. Bu durum, altının elektronlar saçarak kanserli hücrelerin DNA’sına ve sonuçta hücrelerin yapısına zarar vererek kemoterapi ilaçlarının etkisini arttırmasını sağladı.
İşlem çok etkiliydi. Öyle ki, 20 gün sonra hücre kültüründe herhangi bir yeniden canlanma gözlenmedi. Bu da demek oluyordu ki tümör hücreleri tamamen yok edilmişti.
Ancak aynı teknolojinin glioblastomalı hastaların tedavisinde kullanılmasından önce başka çalışmaların yapılması gerekmektedir. Unutulmamalıdır ki alınan sonuçlar gelecekteki tedaviler için yüksek umut barındırmaktadır. Önem arz edecek şekilde, araştırmanın direkt glioblastoma hastalarından alınan hücre hatlarıyla yapılması araştırma ekibine ilaca dirençli tümörlerin evrimi üzerindeki yaklaşımı test etme olanağı vermektedir.
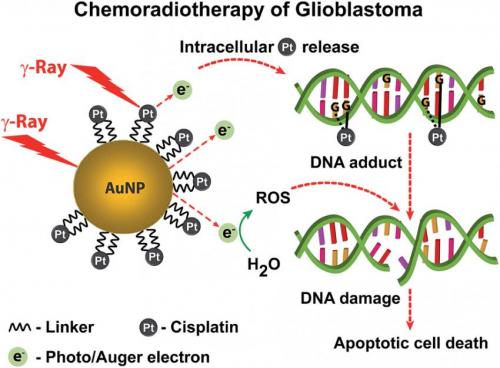 Nano kürenin içeriğini gösteren bir şekil.
Nano kürenin içeriğini gösteren bir şekil.
Bugün çoklu glioblastomanın tedavilere karşı çok dirençli olduğu kanıtlanmıştır. Bunun bir sebebi, tümör hücrelerinin çevrelerini ve sağlıklı beyin dokusunu işgal ederek tümörün cerrahi olarak çıkartılmasını neredeyse imkansız hale getirmesidir.
Kemoterapi ilaçlarının kendi başlarına kullanılması tümör yayılmasının oranını hafifçe azaltabilir. Ancak çoğu durumda hücre populasyonu yenilendikçe, bu geçici etki gösterir. Dolayısıyla, kanserli hücreleri aynı anda doğrudan birden fazla tedaviyle vurmak gerekmektedir. Bu çok önemlidir çünkü bazı kanser hücreleri bir çeşit tedaviye diğerlerinden daha dayanıklıdırlar. Nanoteknoloji sayesinde elde edilen bu fırsatla kanser hücrelerine çifte darbe vurmak ve böylece yeni tedavi seçeneklerinin ortaya çıkması yakın gelecekte gerçekleşecektir.
Tümörleri daha kapsamlı bir şekilde yenmek için bilim insanları altın nanopartiküllerin tedavinin bir noktasında kullanıldığı yeni yollar araştırıyorlar. Altın, hastaya karşı herhangi bir tehlike yaratmadığı için zararsızdır. Ayrıca, altın nanopartiküllerinin büyüklüğü ve şekli istenilen biçimde kontrollü olarak üretilebilir.
Radyoterapiye maruz kaldıklarında partiküller, Auger elektronları olarak bilinen bir çeşit düşük enerji yayarlar. Bu enerji hastalıklı hücrelerin DNA’larına ve başka hücre içi moleküllere zarar verebilir. Bu düşük enerji emisyonu sadece kısa mesafede bir etki gösterir böylece yakınlardaki sağlıklı hücrelerde herhangi bir ciddi zarara yol açmazlar.
Yeni bir çalışmada, araştırmacılar ilk olarak altın nanopartikülleri pozitif yüklü bir polimer olan poliethileniminin içine sardılar. Bu yapı daha sonra hücre yüzeyinde bulunan proteoglikanlarla etkileşime girerek nanopartiküllerin hücre içine alınmasını sağladı.
Bir kere hücre içine girdiklerinde standart radyoterapi kullanılarak uyarılabilen nanopartiküllerin mümkün olması ve sonuçta elektronların salınarak hücre DNA’sına saldırması, çoğu glioblastomalı hasta için bir umut kaynağı olacaktır.
 Nanopartiküller içeren bir kanser hücresi. Resimde hücrenin çekirdeğine (mavi renkli yapı) giren yeşil renkli nanopartiküller gözükmektedir.
Nanopartiküller içeren bir kanser hücresi. Resimde hücrenin çekirdeğine (mavi renkli yapı) giren yeşil renkli nanopartiküller gözükmektedir.
Herhangi eşlik edici bir başka ilaç olmaksızın altın nano kürelerin önemli derecede hücre hasarına neden olduğu bulundu. Ancak tedaviye dayanıklı hücre populasyonunun radyoterapiden sonraki birkaç günde yeniden ortaya çıkmasıyla araştırmacılar sisplatin kaplanmış ikinci bir nano yapı inşa ettiler.
Sisplatinin kemoterapötik etkisi, altın nanopartiküllerinin radyoterapiye duyarlılığı arttıran etkisiyle birleşince oluşan artmış sinerji, hücresel hasarın daha etkili olmasını sağlamaktadır. Sonraki testler muamele edilmeyen hücre kültürlerine kıyasla tedavinin görülen hücre populasyonunu sadece 20 günde 100000 kat azalttığını ortaya çıkarmıştır. Herhangi bir populasyon yenilenmesi belirlenmemiştir.
Araştırmacılar, benzer modellerin en nihayetinde diğer zorlu kanser çeşitleri için de kullanılacağına inanmaktadırlar. Ancak, öncelikli olarak metodun kendisi glioblastomalı hastalar için uygulanabilir bir tedaviye dönüştürülmelidir. Grubun pek çok ileri araştırma yapmasını gerektiren bu süreç aşırı ölçüde testlere ihtiyaç duyacaktır. Ayrıca, nanopartiküllerin en iyi nasıl taşındığının belirlenmesi ve vücudun bu nanopartikülleri güvenli bir şekilde kullanabilmesi için yüzey kimyasının ve büyüklüğünün modifiye edilmesi gibi başka alanlardaki çalışmaların da yapılması gerekmektedir.
Nano bilimcilerle klinikçilerin birlikte çalışmalarıyla optimize edilecek bu yeni tedavi yöntemi, laboratuvardan öte klinikte güçlü etki yaratması bakımından da insanlık için çok önemli bir adım olacaktır.
 Canbolat GÜRSES Genetik ve Nanobiyoteknoloji
Canbolat GÜRSES Genetik ve Nanobiyoteknoloji
